Ⅰ.考察目标
农学门类化学考试涵盖无机及分析化学(普通化学和分析化学)、有机化学等公共基础课程,要求考生比较系统地理解和掌握化学的基础知识、基本理论和基本方法,能够分析、判断和解决有关理论和实际问题。
Ⅱ.考试形式和试卷结构
一、试卷满分及考试时间
本试卷满分为150 分,考试时间为180 分钟。
二、答题方式
答题方式为闭卷、笔试。
三、试卷内容结构
无机及分析化学50% 有机化学50%
四、试卷题型结构
单项选择题30 小题,每小题2 分,共60分
填空题 35空,每空1分,共35 分
计算、分析与合成题 8小题,共55分
Ⅲ.考查范围
无机及分析化学
无机及分析化学考试内容主要包括:化学反应的一般原理、化学平衡、电化学等基础知识;分析误差和数据处理的基本概念,滴定分析、分光光度分析等常用的分析方法。要求考生掌握无机及分析化学的基础知识和基本理论,具有独立分析和解决有关化学问题的能力。
一、溶液和胶体
1.了解分散系的分类及特点。
2.掌握物质的量浓度、物质的量分数和质量摩尔浓度的表示方法及计算。
3.掌握稀溶液依数性的基本概念、计算及其在生活和生产中的应用。
4.掌握胶体的特性及胶团结构式的书写。
5.掌握溶胶的稳定性与聚沉。
二、化学热力学基础
1.了解热力学能、焓、熵及吉布斯自由能等状态函数的性质,功与热等概念。
2.掌握有关热力学第一定律的计算:恒压热与焓变、恒容热与热力学能变的关系及成立的条件。
3.掌握化学反应热、热化学方程式、化学反应进度、标准态、标准摩尔生成焓、标准摩尔生成吉布斯自由能、化学反应的摩尔焓变、化学反应的摩尔熵变、化学反应的摩尔吉布斯自由能变等基本概念及吉布斯判据的应用。
4.掌握化学反应的

的计算。
5.掌握吉布斯一亥姆霍兹方程的计算及温度对反应自发性的影响。
6.掌握化学反应方向的自由能判据。
三、化学反应速率和化学平衡
1.理解化学反应速率、基元反应、复杂反应、反应级数、活化分子、有效碰撞及活化能等基本概念。
2.掌握质量作用定律及化学反应速率方程式的书写。
3.掌握浓度、温度及催化剂对化学反应速率的影响。
4.掌握化学平衡常数的意义及表达式的书写。
5.掌握
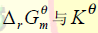
的关系及应用。
6.掌握浓度、压力、温度对化学平衡移动的影响。
7.掌握化学反应等温方程式和平衡常数的有关计算。
8.掌握多重平衡规则。
四、滴定分析概论
1.掌握误差分类与减免方法,精密度与准确度的关系。
2.掌握有效数字及运算规则。
3.掌握滴定分析基本概念和原理、滴定反应的要求与滴定方式、基准物质的条件、标准溶液的配制及滴定结果的计算。
五、酸碱平衡和酸碱滴定法
1.了解质子条件式的书写,掌握弱酸、弱碱和两性物质溶液酸碱度的计算。
2.掌握质子酸、质子碱、稀释定律、同离子效应、共轭酸碱对、解离常数等基本概念。
3.掌握缓冲溶液的类型、配制及有关计算,了解其在农业科学和生命科学中的应用。
4.掌握酸碱指示剂的变色原理,一元酸(碱)滴定过程中pH 的变化规律及常用指示剂的选择。
5.掌握一元弱酸(碱)能否被准确滴定的条件,多元弱酸(碱)能否被分步准确滴定的条件。
6.掌握酸碱滴定的有关计算。
六、沉淀溶解平衡和沉淀滴定法
1.掌握溶度积与溶解度的换算。
2.掌握由溶度积规则判断沉淀的生成与溶解。
3.掌握分步沉淀及其简单应用,了解沉淀转化的条件。
4.了解沉淀滴定法的原理、银量法[莫尔(Mohr)法、佛尔哈德(Volhard)法、法扬司(Fajans)法]滴定终点的确定。
七、氧化还原反应和氧化还原滴定法
1.掌握氧化数、氧化、还原、氧化态、还原态、氧化还原电对、原电池、电极电势、标准氢电极等基本概念。
2.掌握用电池符号表示原电池及原电池电动势的计算。
3.掌握能斯特方程式及浓度(或分压)、酸度对电极电势影响的相关计算。
4.掌握电极电势的应用(判断氧化剂或还原剂的相对强弱,确定氧化还原反应进行的方向、次序和程度)。
5.掌握标准电极电势与氧化还原反应平衡常数的关系。
6.掌握元素标准电势图及其应用。
7.了解氧化还原滴定法的特点,氧化还原指示剂分类。
8.掌握常用的氧化还原滴定方法(重铬酸钾法、高锰酸钾法、碘量法)及氧化还原滴定结果的计算。
八、配位化合物和配位滴定法
1.掌握配合物定义、组成及命名,了解影响配位数的因素。
2.掌握配位平衡与其他平衡的关系,掌握影响配位平衡移动的因素及相关的计算。
3.了解螯合物的结构特点及螯合效应。
4.了解配位滴定法的特点及EDTA的性质。
5.掌握单一金属离子能被准确滴定的条件,配位滴定所允许的最低pH 及提高配位滴定选择性的方法。
6.了解金属指示剂的变色原理,常用指示剂及指示剂使用条件。
7.掌握配位滴定的方式和应用。
九、分光光度法
1.了解分光光度法的基本原理。
2.掌握朗伯一比耳定律的原理、应用及摩尔吸光系数,了解引起偏离朗伯一比耳定律的因素。
3.了解显色反应的特点,掌握显色条件的选择。
有机化学
有机化学考试内容主要包括:有机化合物的命名、结构、物理性质、化学性质、合成方法及其应用;有机化合物各种类型的异构现象;有机化合物分子结构与理化性质之间的关系,典型有机化学反应机制。要求考生掌握有机化学的基础知识和基本理论,具有独立分析解决有关化学问题的能力。
一、绪论
1、掌握有机化合物的结构式及其表示方法;
2、掌握有机化合物中的化学键;
3、了解有机化合物的特性与结构的相关性;
4、了解有机化合物的官能团及其分类。
二、烷烃和环烷烃
1、掌握系统命名的原则、方法;
2、掌握不同类型碳自由基结构与稳定性的关系;
3、掌握环烷烃的结构和性质;
4、了解构象的概念、产生原因及各种不同构象的稳定性;
5、了解自由基反应机制。
三、 烯烃、炔烃和二烯烃
1、掌握烯烃、炔烃和二烯烃的化学性质;
2、掌握亲电加成反应历程;
3、掌握产生顺反异构的原因和条件,顺反异构体的命名;
4、了解诱导效应和共轭效应产生的原因、特点及反应部位与结构的相关性;
5、了解诱导效应和碳正离子的稳定性对加成反应取向的解释;
四、 芳香烃
1、掌握苯的结构、芳香性及Huckel 规则;
2、掌握苯的化学性质;
3、掌握芳环上亲电取代反应的定位规律;
4、了解芳香性概念和芳香性化合物的结构特点;
5、了解芳环亲电取代反应机理。
五、 旋光异构
1、掌握旋光异构的概念、构型及构型标记;
2、掌握手性分子的判断、含手性碳原子化合物的旋光异构;
3、了解旋光性与分子结构的关系;
4、了解环状化合物和不含手性碳原子的手性分子结构。
六、 卤代烃
1、掌握卤代烃的化学性质;
2、掌握卤代烯烃和卤代芳烃的结构与性质的相关分析;
3、掌握亲核取代反应的SN1、SN2 机理及立体化学特征;
4、了解卤原子的活性与结构的关系;
5、了解消除反应的E1、E2机理及立体化学特征。
七、 醇、酚、醚
1、掌握醇、酚、醚的分类、结构和命名;
2、掌握醇、酚、醚的化学性质;
3、了解醇、酚、醚的物理性质;
4、了解醇、酚、醚的结构与性质的关系。
八、 醛、酮
1、掌握醛、酮的结构、分类和命名;
2、掌握羰基结构特点和亲核加成反应及其历程;
3、掌握醛、酮的化学性质及某些性质在分析、鉴定和生化过程中的意义;
4、了解醛、酮的物理性质。
九、 羧酸及其衍生物和取代酸
1、掌握羧酸、羧酸衍生物、取代酸的分类、结构和命名(包括重要羧酸的俗名);
2、掌握羧酸及其羧酸衍生物化学性质;
3、了解羧酸、羧酸衍生物、取代酸的物理性质;
4、了解互变异构现象。
十、 含氮有机化合物
1、掌握胺的结构、分类和命名;
2、掌握胺的化学性质;
3、掌握重氮盐的生成及在合成上的应用;
4、了解胺的碱性强弱比较及原因。
十一 、杂环化合物
1、掌握主要的杂环结构和名称;
2、掌握呋喃、吡咯、噻吩、吡啶的结构与芳香性的关系,结构与亲电取代反应活性的关系;
3. 掌握几种常见的重要杂环化合物的化学性质。
主要参考书:
普通化学:《普通化学》(第二版).王春娜、石军主编.中国农业出版社(ISBN978-7-109-19950-7)
分析化学:《定量分析化学》(第一版).葛兴、石军主编.中国林业出版社(ISBN978-7-5038-6424-7)
有机化学:《有机化学》(第三版).赵建庄、尹立辉主编. 中国林业出版社(ISBN978-7-5038-7248-8)
购买天津高校考研专业课资料请点击:http://www.52kaoyan.com/Shop/data/



















